Un peu d'histoire
Les origines de la cryogénie...

Il y a moins dĺun centenaire que nous produisons
sur mesure du froid, auparavant, il fallait attendre lĺhiver pour emmagasiner
des blocs de glace dans des bâtiment appelées «áglacièresá».
|
Il y a des dizaines de milliers dĺannées, lĺhomme passait dĺun état nomade, étant sans cesse à
lĺaffût dĺun meilleur territoire de chasse, à un état sédentaire. Au lieu dĺaller vers ses proies,
lĺhomme les domestiquait afin de minimiser ses déplacements. Et, déjà à cette époque, lĺhomme avait
aussi apprivoisé lĺusage du feu. Outre la chaleur et la lumière quĺil procure, le feu servit dès lors
à lĺamélioration de lĺoutillage. Donc, très tôt dans son histoire, lĺhomme a maîtrisé plusieurs
applications impliquant de hautes températures.
Lĺutilisation de basses températures, quant à elle, restait fort méconnue.
En fait, le froid nĺexistait quĺen hiver, au sommet des montagnes ou dans
certaines grottes bien spéciales, les glacières naturelles. Celles-ci
produisaient même de la glace en été. Mais avant la venue des
réfrigérateurs, la plupart des gens conservait leurs aliments en sĺapprovisionnant
en glace chez un marchand, qui, durant lĺhiver près dĺune étendue dĺeau gelée, la
coupait et la transportait dans une glacière, un bâtiment bien isolé thermiquement.
Il pouvait ainsi en vendre durant tout lĺété. |
Avant de pouvoir produire artificiellement du froid, il a fallu tout dĺabord maîtriser
le concept de température et produire des instruments aptes à la mesurer. Une étape
importante en ce sens fut lĺinvention du thermomètre à mercure par Gabriel Fahrenheit,
en 1720. Considéré comme un appareil de luxe, le thermomètre devient un instrument
indispensable à lĺavancement de la thermodynamique, lĺétude de la température et de la
chaleur. Entre autres, les scientifiques sĺaperçurent que les changements dĺétat
(par exemple, passer de lĺétat solide à liquide ou vice-versa) des éléments simples
sĺeffectuent toujours à la même température et ce, tant que la pression demeure constante.
Par simplicité, Anders Celsius réorganise lĺéchelle Fahrenheit pour lui attribuer
des valeurs plus faciles à retenir. Il attribua 0°C au point dĺébullition de
lĺeau et 100°C au point de con.gélation. Heureusement, aujourdĺhui nous utilisons
une convention plus intuitive où 0°C correspond au point de fusion de lĺeau et 100°C
au point dĺébullition.
Par la suite, lĺutilisation du thermomètre permit aux physiciens de découvrir, sur
une période de plus de cinquante années de recherche intensive, une relation unissant
à la fois la température (T), la pression (P) et le volume (V) dĺun gaz :
PV = nR (T+A)
et où A représente une constante qui vaut approximativement ľ270°C. Cette relation,
est connue sous le nom dĺéquation des gaz parfaits.
|
|
Les physiciens firent, avec la découverte de cette relation, un pas de plus vers la
domestication du froid. Comme une variation du volume ou de la pression influe sur la
température, il devenait possible dĺabaisser la température du gaz. Cependant, avant
de pouvoir vérifier cette prédiction, il fallut encore un bon nombre dĺannées de recherche.
Au cours de cette période, sĺétablirent les bases théoriques de la thermodynamique :
formule de Regnault, cycles de Carnot, diagramme de Clapeyron et bien dĺautres.
De plus, lĺéquation des gaz parfaits suggéra aux physiciens lĺexistence dĺune température
limite en deçà de laquelle la réfrigération dĺun gaz devenait impossible. En effet,
un abaissement de température provoque, à volume fixe, un abaissement de la pression.
Or, la pression dĺun gaz ne peut pas logiquement devenir négative. De même, à pression fixe,
une diminution de la température provoque une diminution de volume, mais celui-ci ne peut
pas non plus devenir négatif. Certains physiciens, comme Gay-Lussac, tentèrent donc de trouver
théoriquement la température limite qui correspondait à un volume nul. Ils obtinrent une
valeur équivalente à environ -270°C. Dès lors, les scientifiques devinrent convaincus que
la température dĺun gaz ne peut sĺabaisser en dessous de cette valeur, car si tel était le
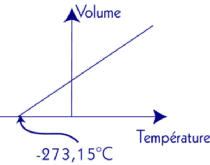
cas, le volume dĺun gaz deviendrait négatif (voir graphique). Lord Kelvin conçu alors une
nouvelle échelle de température plus appropriée à lĺétude des phénomènes en basses
températures puisquĺelle éviterait des valeurs trop encombrantes. Par ce choix judicieux,
on dit maintenant : «áun réfrigérateur à dilution (voir plus loin) peut atteindre des
températures de lĺordre de 5mK (0,005K)á» plutôt que -273,145°C, plus fastidieux. Plus
fondamentalement, Kelvin posa vers 1850, que le zéro de son échelle correspondrait à la
valeur théorique la plus basse possible. |
Graphique mettant en relation le volume et la température dĺun gaz à pression constante.
|
Quelques années auparavant, on sĺétait aperçu que la compression dĺun gaz augmentait sa température,
alors que sa décompression provoquait un refroidissement. En abaissant la pression à lĺintérieur
dĺune seringue, par exemple, on diminue la température de lĺair. Mais lĺétanchéité imparfaite et la
basse pression interne font en sorte que de lĺair ambiant pénètre dans la seringue, augmentant ainsi
peu à peu la température et annulant lĺeffet obtenu. Cependant, ce petit pépin ne gêna en rien les
scientifiques qui sĺacharnaient inlassablement sur la question du froid. Pour contrer astucieusement
le problème, ils comprimèrent dĺabord lĺair, puis attendirent son refroidissement à la température de
la pièce. Ensuite, ils décompressèrent subitement le gaz baissant ainsi sa température de quelques
degrés. Cette opération se déroulait à la pression atmosphérique.
|
Lord Kelvin
Gracieuseté de l' Université de St-Andrews, Écosse |
Vers le milieu du XIXe siècle, un tel procédé réalisé cycliquement permit aux physiciens de créer
artificiellement, et ce, pour la toute première fois, de la glace. Cependant, les chercheurs ne
sĺarrêtèrent pas seulement à la congélation de lĺeau. Ils tentèrent de faire subir les plus fortes
décompressions techniquement possibles aux gaz sans toutefois pouvoir franchir -40°C. À cette
température, ils purent liquéfier le chlore et solidifier lĺeau mais sans plus. La course pour
lĺamélioration des techniques de refroidissement se mit alors en branle. Plusieurs chercheurs
reprenaient lĺexpérience en y changeant certains aspects afin dĺaméliorer la chute de température
finale. Chacune des nouvelles innovations techniques permettait dĺatteindre de nouvelles limites
thermiques, mais personne nĺavait encore réussi à liquéfier lĺair, le mélange de gaz le plus abondant
sur Terre. |
En 1877, Pictet se servit de la détente Joule-Thomson, une détente lente sans échange de chaleur avec
lĺenvironnement au cours de laquelle le gaz, en augmentant de volume, effectue un travail sur un piston.
Ce type de détente, qui évite la formation de tourbillons dans le gaz, minimise le «ádésordreá». Cette
détente se produit à entropie presque constante (sans grande augmentation du désordre) et produit
un meilleur refroidissement. Par ce moyen, Pictet réussit à obtenir un brouillard dĺair, semblable aux
fines gouttelettes en suspension observables parfois à lĺaube. Cependant, la liquéfaction de lĺoxygène
(90,3 K) dut attendre encore six années complètes. Ensuite, à peine quelques années suffirent pour être
en mesure de liquéfier le krypton (120 K), le fluor (85 K), lĺargon (87 K) et lĺazote (77 K) qui furent
respectivement découverts par Sir William Ramsey, Joseph Henri Moissan, W. Ramsey et Daniel Rutherford.
Deux gaz résistaient néanmoins à la fameuse liquéfactioná: lĺhydrogène et lĺhélium. Ces gaz rebelles
contredisaient la théorie de lĺépoque : les physiciens croyaient que tous les éléments pouvaient, sous
certaines conditions de pression et de température, se retrouver sous les trois phases : lĺétat solide,
liquide ou gazeux. Ainsi, à la fin du XIXe siècle, les savants considéraient que ces deux gaz dérogeaient
à la théorie. Mais, en 1898, la mise au point dĺune technologie permettant une détente adiabatique
(à entropie constante, cĺest-à-dire, sans ajout de désordre), permit à Dewar de liquéfier lĺhydrogène
à 20,3 K et, en 1908, à Kamerlingh-Onnes de liquéfier lĺhélium à 4,2 K.
Une fois que la grande majorité des gaz connus furent ainsi liquéfiés, les physiciens tentèrent de sĺapprocher
le plus près possible du zéro absolu. Malheureusement, à des températures aussi basses que quelques dizaines
de degrés Kelvin, les cryostats ne résistaient pas : les soudures se brisaient, le métal se fendait et le matériel
utilisé pour le refroidissement devenait alors inutilisable. La mise au point de certains alliages fort complexes,
qui résistent mieux aux basses températures, a nécessité de nombreuses années de recherche. Toutefois, à chaque
percée, les mêmes problèmes réapparaissent lorsque lĺon tente de se rapprocher davantage du zéro absolu. Bien que
la technologie se soit énormément améliorée au cours du dernier siècle, il reste quĺaux très basses températures,
le matériel utilisé en laboratoire se fragmente souvent.
Dans les multiples laboratoires du monde, la course vers le zéro absolu continue. Aujourdĺhui, lĺhomme
dépasse la nature en matière de froid, puisque des réfrigérateurs atteignent des températures plus froides
que lĺespace intersidéral. En effet, une équipe de physiciens située dans la ville de Bayreuth réussit,
en 1988, à abaisser la température de 127 grammes de cuivre à 1,2 Î 10-5 K, soit environ 105 fois inférieur
à la température moyenne de lĺUnivers, qui avoisine les 2,7áK. Pour y arriver, ces chercheurs mirent au
point le cryostat à dilution qui utilise certaines propriétés quantiques propres à lĺatome dĺhélium aux
basses températures (voir La cryogénie à Sherbrooke).
Mais les chercheurs ne sĺarrêtèrent pas là. Ils se servirent par la suite de phénomènes magnétiques et
parvinrent à se rapprocher encore plus de la limite théorique sans toutefois lĺatteindre. La désaimantation
adiabatique (voir Désaimantation adiabatique) a permis de refroidir un échantillon au voisinage de 10-9 K.
|
Une vision microscopique au zéro absolu
Dans lĺhistoire de la physique, il arrive quelquefois, bien quĺon assiste généralement au
contraire, que la théorie dépasse la technologie. Autrement dit, les physiciens comprennent
théoriquement les causes dĺun phénomène, mais ne peuvent pas vérifier expérimentalement leur
acquis théorique. Lĺhistoire de la cryogénie suit ce schéma. Dès le début du XXe siècle, la
thermodynamique avancée par les physiciens expliquait la température dĺun corps par lĺagitation
de ses particules. La limite théorique du zéro absolu prit alors une toute autre signification :
elle correspondrait à lĺimmobilisation des particules. Mais, une théorie naissante allait tout
remettre en question. Selon la physique quantique (voir LĺAttracteur No 12), on ne peut pas
connaître à la fois la vitesse et la position précise dĺune particule. Or, affirmer quĺune
particule au zéro Kelvin sĺimmobilise, revient à contredire directement le principe dĺHeisenberg
puisque, dans un tel cas, nous connaîtrions exactement la position (stable) et la vitesse
(nulle) de la particule. Maintenant, selon la vision des physiciens, au zéro absolu, chaque
particule occupe le niveau dĺénergie le plus bas.
|
|
Lĺhydrogène liquide, qui ne trouvait aucune application pratique au début du siècle,
a aujourdĺhui une place importante en aérospatiale : il sert de carburant aux décollages de fusées spatiales.
|
Remarque : plus on réduit la valeur résiduelle de la température, plus il est difficile de retrancher,
disons 50% de cette température. Par exemple, il est plus facile de passer de 2 à 1 degrés Kelvin que
de sauter de 1 à ½ degré Kelvin. Le zéro absolu constitue, en quelque sorte, une limite théorique
infranchissable. En 1913, Walter Nernst, prix Nobel en 1920, a établi quĺon ne pourrait jamais
atteindre le zéro absolu. Cela fait penser à la vitesse de la lumière. Tout comme un objet requiert
un apport dĺénergie toujours plus grand pour sĺapprocher de la vitesse de la lumière, sans toutefois
pouvoir lĺatteindre, abaisser un échantillon à une température avoisinant le zéro absolu nécessite
des moyens toujours plus extraordinaires. Aujourdĺhui, les températures les plus basses sont obtenues
en refroidissant des gaz à lĺaide de lasers, mais ces techniques ne permettent pas de refroidir une grande
quantité de matière.
Les progrès technologiques acquis au cours du dernier siècle permettent dĺatteindre des températures
beaucoup plus basses quĺautrefois. Lĺabaissement des coûts de production des liquides cryogéniques a
permis dĺen faire un commerce lucratif. Moins cher que lĺessence, ces liquides servent principalement
aux lancements de fusées et à la recherche.
|
Pourquoi, vous demanderez-vous, sĺacharner ainsi à atteindre des températures toujours plus basses si
les scientifiques savent cette quête du zéro absolu utopique? Parce que la recherche en basse température
a permis de révéler certains secrets, jusque là inconnus, sur le comportement et la composition de la matière.
La supraconductivité, qui correspond à une chute brutale de la résistance électrique, et la superfluidité
de certains liquides, qui coulent sans résistance et défient la gravité en remontant les parois des contenants
où ils reposent, ont été découvertes grâce à lĺétude du froid. Ni un fantasme de scientifiques isolés, ni
dénuée de sens, la quête incessante vers lĺatteinte du zéro absolu sert à comprendre le comportement de la
matière à température ambiante à partir de constatations et de découvertes ne se révélant quĺà basses
températures. Les températures extrêmes (10-9 K) ne contribuent pas encore à lĺéconomie à grande échelle,
mais qui sait ce que nous réserve lĺavenir? Pensons aux liquides cryogéniques à leur début. Sans
application utile, leur production stagna pendant plusieurs années. Aujourdĺhui, ces liquides,
indispensables à lĺhomme, lui permettent de voyager dans lĺespace (carburants pour les fusées) et
dĺexplorer le vivant en refroidissant les supraconducteurs des appareils dĺimagerie par résonance
magnétique. Les applications pratiques des températures records verront, elles aussi, le jour et,
espérons-le, amélioreront notre condition humaine.
|
La supraconduction,
lĺune des nombreuses
applications de la cryogénie. |
LCD f
_________________________________________________
Bibliographie
- Un site Internet sur les glacières naturelles
- Toujours plus froid : un nouveau pas dans la recherche des très basses températures, Sciences et vie, août 1988, p. 12-13
Photographies